Введите слово или словосочетание на любом языке 👆
Язык:
Перевод и анализ слов искусственным интеллектом ChatGPT
На этой странице Вы можете получить подробный анализ слова или словосочетания, произведенный с помощью лучшей на сегодняшний день технологии искусственного интеллекта:
- как употребляется слово
- частота употребления
- используется оно чаще в устной или письменной речи
- варианты перевода слова
- примеры употребления (несколько фраз с переводом)
- этимология
Что (кто) такое Третье начало термодинамики - определение
ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ
(Нернста теорема) , устанавливает, что энтропия физической системы при стремлении температуры к абсолютному нулю не зависит от параметров системы и остается неизменной. М. Планк дополнил теорему Нернста гипотезой, что энтропия всех тел при абсолютном нуле температуры равна нулю. Из третьего начала термодинамики вытекают важные следствия о свойствах веществ вблизи абсолютного нуля. Так, обращаются в нуль: удельные теплоемкости при постоянном объеме (Сv) и при постоянном давлении (Сp), термический коэффициент расширения и давления. Из третьего начала термодинамики следует также недостижимость абсолютного нуля температуры при конечной последовательности термодинамических процессов.
Третье начало термодинамики
тепловой закон Нернста (Нернста теорема), закон термодинамики, согласно которому Энтропия S любой системы стремится к конечному для неё пределу, не зависящему от давления, плотности или фазы, при стремлении температуры (Т) к абсолютному нулю (В. Нернст, 1906). Т. н. т. позволяет находить абсолютное значения энтропии, что нельзя сделать в рамках классической термодинамики (на основе первого и второго начал термодинамики). В классической термодинамике энтропия может быть определена лишь с точностью до произвольной аддитивной постоянной S0, что практически не мешает большинству термодинамических исследований, так как реально измеряется разность энтропий (S0) в различных состояниях. Согласно Т. н. т., при Т → 0 значение ΔS → 0.
В 1911 М. Планк сформулировал Т. н. т. как условие обращения в нуль энтропии всех тел при стремлении температуры к абсолютному нулю: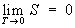 . Отсюда S0 = 0, что даёт возможность определять абсолютное значения энтропии и др. потенциалов термодинамических (См. Потенциалы термодинамические). Формулировка Планка соответствует определению энтропии в статистической физике (См. Статистическая физика) через термодинамическую вероятность (W) состояния системы S = klnW (см. Больцмана принцип). При абсолютном нуле температуры система находится в основном квантово-механическом состоянии, если оно невырождено, для которого W = 1 (состояние реализуется единственным микрораспределением). Следовательно, энтропия S при Т = 0 равна нулю. В действительности при всех измерениях стремление энтропии к нулю начинает проявляться значительно раньше, чем может стать существенной при T → 0 дискретность квантовых уровней макроскопической системы, приводящая к явлениям квантового вырождения.
. Отсюда S0 = 0, что даёт возможность определять абсолютное значения энтропии и др. потенциалов термодинамических (См. Потенциалы термодинамические). Формулировка Планка соответствует определению энтропии в статистической физике (См. Статистическая физика) через термодинамическую вероятность (W) состояния системы S = klnW (см. Больцмана принцип). При абсолютном нуле температуры система находится в основном квантово-механическом состоянии, если оно невырождено, для которого W = 1 (состояние реализуется единственным микрораспределением). Следовательно, энтропия S при Т = 0 равна нулю. В действительности при всех измерениях стремление энтропии к нулю начинает проявляться значительно раньше, чем может стать существенной при T → 0 дискретность квантовых уровней макроскопической системы, приводящая к явлениям квантового вырождения.
Из Т. н. т. следует, что абсолютного нуля температуры нельзя достигнуть ни в каком конечном процессе, связанном с изменением энтропии, к нему можно лишь асимптотически приближаться, поэтому Т. н. т. иногда формулируют как принцип недостижимости абсолютного нуля температуры. Из Т. н. т. вытекает ряд термодинамических следствий: при T → 0 должны стремиться к нулю теплоёмкости при постоянном давлении и при постоянном объёме, коэффициенты теплового расширения и некоторые аналогичные величины. Справедливость Т. н. т. одно время подвергалась сомнению, но позже было выяснено, что все кажущиеся противоречия (ненулевое значение энтропии у ряда веществ при Т = 0) связаны с метастабильными состояниями (См. Метастабильное состояние) вещества, которые нельзя считать термодинамически равновесными.
Лит.: Клейн М., Законы термодинамики, в сборнике: Термодинамика необратимых процессов. Лекции в летней международной школе физики им. Э. Ферми, пер. с англ., М., 1962. См. также лит. при статьях Термодинамика и Статистическая физика.
Д. Н. Зубарев.
Третье начало термодинамики
Третье начало термодинамики (теорема Нернста, тепловая теорема Нернста) — физический принцип, определяющий поведение энтропии при приближении температуры к абсолютному нулю. Является одним из постулатов термодинамики, принимаемым на основе обобщения значительного количества экспериментальных данных по термодинамике гальванических элементов. Теорема сформулирована Вальтером Нернстом в 1906 году. Современная формулировка теоремы принадлежит Максу Планку.
Википедия
Третье начало термодинамики
Третье начало термодинамики (теорема Нернста, тепловая теорема Нернста) — физический принцип, определяющий поведение энтропии при приближении температуры к абсолютному нулю. Является одним из постулатов термодинамики, принимаемым на основе обобщения значительного количества экспериментальных данных по термодинамике гальванических элементов. Теорема сформулирована Вальтером Нернстом в 1906 году. Современная формулировка теоремы принадлежит Максу Планку.

